 |
BRC Current Technology August 2021 |
17. CRISPR/Cas9で高効率に
| |
 |
|
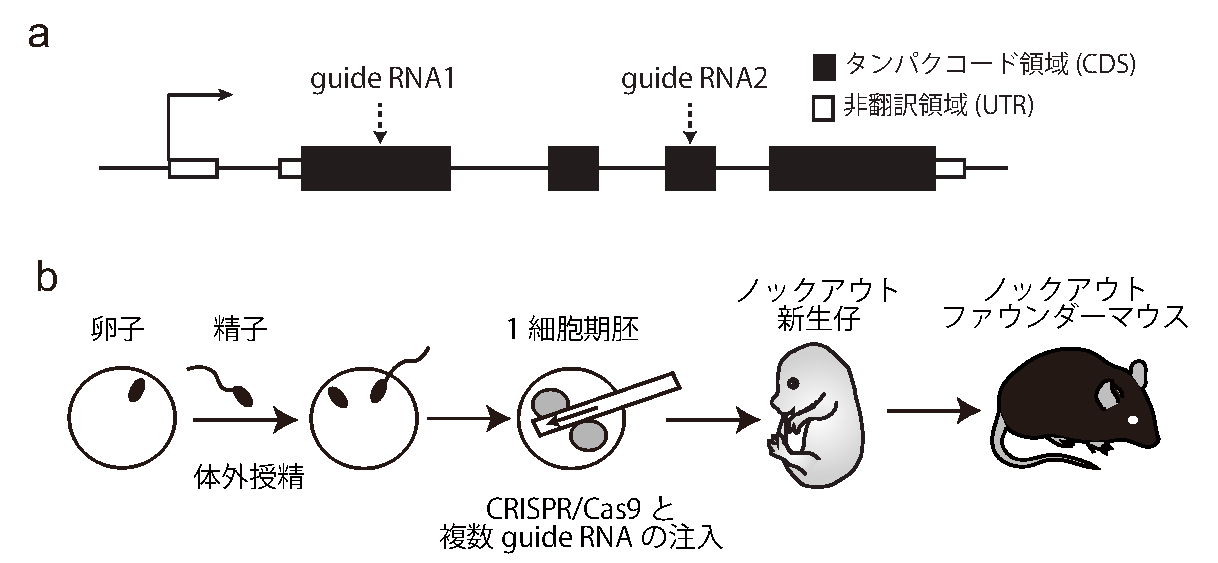
| 図1. CRISPRによるノックアウト(KO)ファウンダーマウスの作製法。 | |
| (a) | タンパクをコードするエクソンの異なる2か所以上に対してguide RNAをデザインする。 |
| (b) | 上記のようにしてデザインした複数のguide RNAをCas9 mRNAと同時に受精卵に注入すると、 非常に高い効率(95-100%)で遺伝子の機能を破壊できる。 |
 |
|
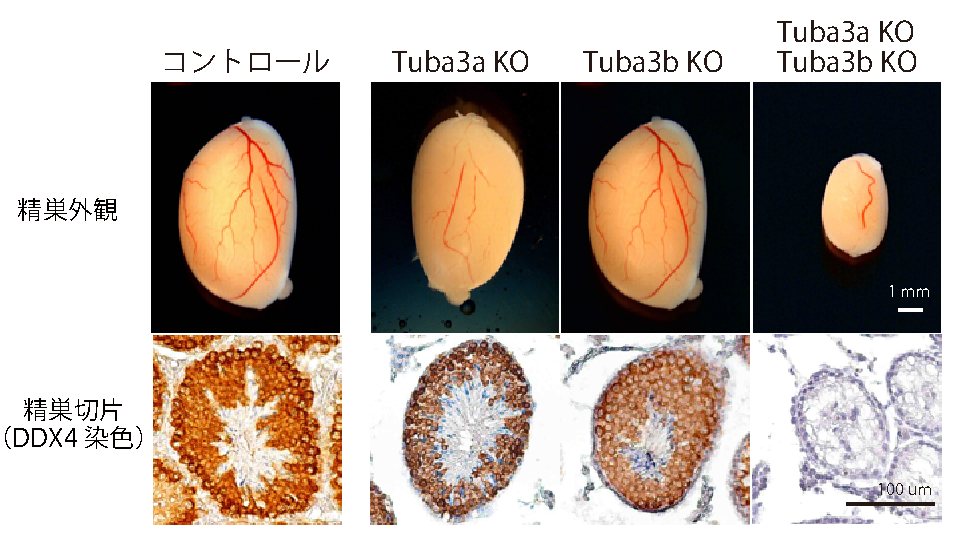
| 図2. Tuba3aとTuba3b遺伝子の同時破壊によって起こる生殖細胞発生異常。 | |
| Tuba3a、Tuba3bそれぞれ単独KOしたファウンダーマウスは特に異常を示さないが、2遺伝子を同時に破壊したダブルKOファウンダーマウスでは精巣が顕著に委縮しており、DDX4陽性の生殖細胞が完全に消失していた。 | |
| これまでノックアウトマウスの表現型解析アプローチでは、ファウンダーマウスを交配により系統化したうえで、ヘテロ個体同士の交配を介してノックアウトマウスを作製してきました。このようなアプローチではファウンダー作製の後も数世代の交配を必要とするため、解析に非常に長い時間がかかっていました。CRISPR/Cas9法は高効率にターゲット領域のゲノムを編集できる革新的な技術です。これまで、CRISPR/Cas9のguide RNAを1遺伝子に対して複数同時に注入することで、高い効率で両アレルに変異の入ったノックアウトファウンダーマウスを作製できることが報告されています[1]。我々もこのアプローチによって、ほぼ100%の効率でノックアウトファウンダーマウスを作製することに成功してきました[2]。今回、この手法を2遺伝子に対して同時に使用することで、2遺伝子のダブルKOファウンダーマウスを直接作製することに成功しました[3]。Tuba3aとTuba3b遺伝子を同時破壊した結果、精巣の生殖細胞が完全に消失することが明らかになりました。このような複数遺伝子の同時破壊は、これまでの交配をベースとしたアプローチと比べて格段に時間を短縮できるため、表現型スクリーニング法として非常に有用であると考えられます。 | |
| References: | [1] | E. A. Susaki et al., “Next-generation mammalian genetics toward organism-level systems biology,” npj Sys. Biol. Appl., 3, 1–10, 2017. |
| [2] | S. Matoba et al., “Paternal knockout of Slc38a4/SNAT4 causes placental hypoplasia associated with intrauterine growth restriction in mice,” Proc. Natl. Acad. Sci. U. S. A., 116, 21047–21053, 2019. |
|
| [3] | M. S. Akter et al., “CRISPR/Cas9-based genetic screen of SCNT-reprogramming resistant genes identifies critical genes for male germ cell development in mice,” Sci. Rep., DOI: 10.1038/s41598-021-94851-9, 2021. |




